Erisoojus
|
Erisoojus on soojushulk kalorites, mis on vajalik 1g aine temperatuuri tõstmiseks 1°C võrra. Vee erisoojus on väga suur (1,0) ning sellest suurem erisoojus on vaid vedelal ammoniaagil (1,23), vedelal vesinikul (3,4) ja liitiumil. Teistel biosfääri komponentidel on erisoojus palju väiksem. Näiteks kivimitel on see ligikaudu 0,2. Vee suure erisoojuse ja aurustumissoojuse põhjuseks on asjaolu, et vee molekulide vahel olevate vesiniksidemete lõhkumiseks on vaja suhteliselt palju energiat. Vee suur soojusmahtuvus loob hüdrosfääris hoopis stabiilsema keskkonna kui maismaal (Joonis 6).
|
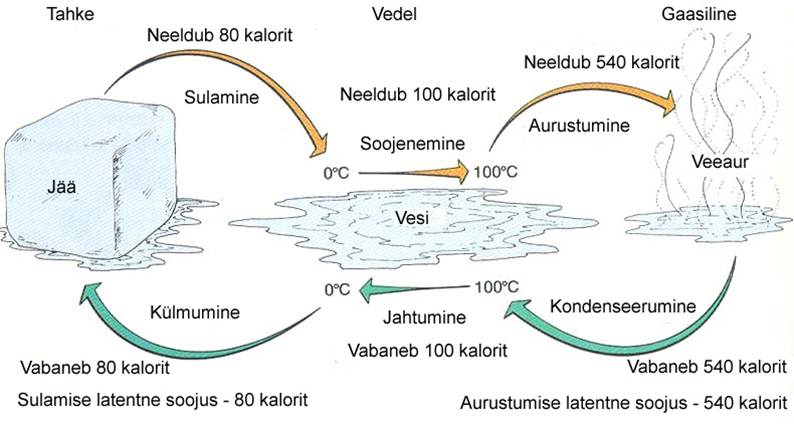
Temperatuurikõikumised toimuvad aegamööda ning päevased ja sesoonsed temperatuurierinevused on tunduvalt väiksemad kui õhkkeskkonnas. Vette salvestunud suured soojushulgad avaldavad mõju ka kliimale. Näiteks Atlandi ookeani soe Golfi hoovus parandab märkimisväärselt Lääne-Euroopa klimaatilisi tingimusi. Jää erisoojus on 0°C juures umbes pool vee omast (0,5 cal·gˉ¹·°Cˉ¹) ja see väheneb progressiivselt temperatuuri langedes. Samas on jää sulatamiseks vajalik energiahulk suur (sulamissoojus 79,72 cal·gˉ¹) ning veel suurem on vee aurustumissoojus (540 cal·gˉ¹) (Joonis 7).
Veeauru veeldumisel aga vabaneb uuest 540 cal·gˉ¹. Ja vastupidiselt, 0°C juures oleva vee jäätumisel vabaneb omakorda jällegi 79,72 cal·gˉ¹. Nende omaduste tõttu on kevadeti vaja suurel hulgal energiat jää sulatamiseks ja sama suurel hulgal energiat vabaneb sügisel jäätumisel. Seepärast on veekogude läheduses kevadel alati jahedam ja sügisel soojem.