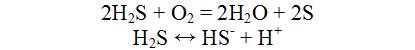Väävelvesinik
Vees lahustub väävelvesinik (H2S) väga hästi. H2S lahustuvus on 0° C juures 4370 ml/l. Ehk siis tihedust (1,393) arvestades ca 6000 mg/l. Vesiniksulfiid oksüdeerub kergesti molekulaarse hapniku mõjul ning dissotsieerub vees:
Reaktsioon on pH-sõltuv, väävelvesinik esineb loodusvetes vaid madala pH juures, pH tõustes on ülekaalus juba sulfiidid. Veekogudes moodustub väävelvesinik eranditult biogeensel teel (sulfaatide redutseerimine ja orgaanilise väävli lagundamine) mitmesuguste bakterite elutegevuse tulemusena.
|
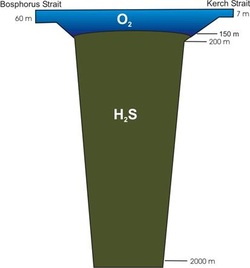
Seda tarbivad ka värvitud ja rohelised ning purpursed väävlibakterid (Joonis 28). Sulfaatide redutseerimine toimub kui redokspotentsiaal < 100 mV. H2S on vee-elustikule mürgine juba väikestes kogustes. Väävelvesiniku mürgisus on võrreldav vesiniktsüaniidi omaga ning toksilisus on seotud mitkondriaalses tsütokroomis oleva rauaga kompleksühendi moodustamises. Mustas meres on näiteks selle gaasi tõttu elutud (leiduvad ainult prokarüoodid) piirkonnad, mis on sügavamal kui 150-250 m (Joonis 29). Olulisel määral on küllastunud näiteks Kaspia mere või Norra fjordide põhjakihid. Ka kihistunud liig- ning rohketoiteliste väikejärvede hüpolimnioni koguneb talvise või suvise stagnatsiooniperioodi jooksul tihti väga suurtes kogustes väävelvesinikku, millest vabanemine toimub kevadise-sügisese segunemise ajal. Vastupidiselt väävelvesinikule pole sulfiidid vee-elustikule mürgised. Sulfiidide hulk järves ja nende dünaamika sõltub oluliselt raua- ja mangaanivarudest, sest nende sulfiidid on lahustumatud ja langevad sademena välja.
|