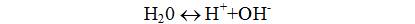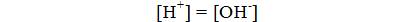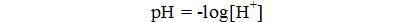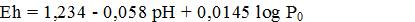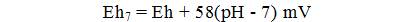pH ja redokspotentsiaal
Destilleeritud vesi on äärmiselt nõrk elektrolüüt. 556 miljoni vee molekuli kohta dissotsieerub üks molekul vett:
Vesi dissotsieerub üheaegselt kui hape ja kui alus, tal on võrdselt nii happelised kui ka aluselised omadused. Et vee molekulide dissotsiatsioonil tekib võrdne arv vesinik- ja hüdroksiidioone, siis on puhtas vees nende kontsentratsioon (10^7 mooli ioone/l) võrdne:
ning keskkonna reaktsioon neutraalne. Happelises lahuses ületab vesinikioonide kontsentratsioon hüdroksiidioonide kontsentratsiooni, aluselises keskkonnas aga hüdroksiidioonide kontsentratsioon suurem kui vesinikioonidel. Praktikas on aga võrdlemisi ebamugav kasutada ülaltoodud kontsentratsiooni väljendust. Seepärast kasutatakse keskkonna happelisuse või aluselisuse hindamisel negatiivset kümnendlogaritmi vesinikioonide kontsentratsioonist. Seda nimetatakse vesinikeksponendiks ja tähistatakse pH:
Ehk siis neutraalne pH on 7 ja happeline< 7 ning aluseline >7.
|
Looduslikes vetes on vesinikioonide kontsentratsioon karbonaatse puhversüsteemi tõttu suhteliselt püsiv. Karbonaatide puudumisel ja süsihappegaasiga küllastumisel võib pH langeda 5,67ni. Rabajärvede pH on turbasammalde tugeva ioonvahetusvõime ja humiinainete rohkuse tõttu enamasti 3-4. Vulkaaniliselt aktiivsetes piirkondades asuvates järvedes võib pH veelgi madalam olla (Joonis 36), kuna vulkaanilised gaasid, reageerides veega moodustavad väga tugevaid happeid. Rohketoitelistes veekogudes võib intensiivse fotosünteesi korral aga pH tõusta üle 10, kuna vees praktiliselt puudub vaba süsihappegaasi (Joonis 37). Merevee pH on enamasti vahemikus 8,1-8,4.
|
|
Tihti võib ühes ja samas veekogus pH ööpäeva jooksul kõikuda 2 või rohkema ühiku võrra. Öösel langeb pH tänu hingamisel vabaneva CO2 tõttu, päeval aga tõuseb, kuna taimed tarbivad süsihappegaasi. Järvede ja sooveekogude põhjasetete pH ei tõuse tavaliselt üle 7, küll aga on seda meresetete oma, eriti hästi väljakujunenud hoovuste piirkonnas.
|
pH on oluliseks keskkonnafaktoriks, mõjutades veeorganismide ensüümide tööd, membraantranspordi toimumist ja ka membraane endid. Tundlikkuse suhtes pH muutustesse jaotatakse hüdrobiondid kahte rühma. Stenoioonsed organismid ei talu suuri pH kõikumisi ja elavad vetes, kus pH muutused ei ületa reeglina viite ühikut. Eurüioonsed organismid taluvad aga palju suuremat pH vahemikku ning võivad elada nii happelises kui ka aluselises keskkonnas. Eurüioonsete loomade näiteks võiks olla perekonna Chironomus vastsed (Joonis 38), mis väidetaval taluvad pH vahemikku 2-10. Sõltuvalt keskkonnatingimustest jagatakse stenoioonsed organismid omakorda kahte rühma. Atsidofiilid e. happelist keskkonda eelistavad ning alkalifiilid e. aluselist keskkonda eelistavad. Tüüpilised alkalifiilide esindajad on näiteks limused ja koorikloomad.
|
Kui pH sõltub aluseliste ja happeliste ainete vahekorrast vees, siis redokspotentsiaal sõltub muutuva valentsiga elementide esinemissagedusest vees. Analoogselt happe-aluse tasakaalule, mida iseloomustab pH, on loodusvetele iseloomulik redokstasakaal, mida iseloomustab siis redokspotentsiaal. Kui pH oli negatiivne logaritm vesinikioonide kontsentratsioonist, siis pE on negatiivne logaritm elektronide aktiivsusest. pE on mõõtühikuta suurus, mis iseloomustab keemilise süsteemi võimet vahetada elektrone ja seal toimuvaid redoksreaktsioone. pE on negatiivne redutseerivates tingimustes ja positiivne oksüdeerivates tingimustes. Redokspotentsiaali mõõdetakse millivoltides ning tähiseks on Eh või lihtsalt E:
Redutseerivate tingimuste juures on Eh või pE madalad (Eh –300 kuni –100 mV, pE –15 kuni –5) ja oksüdeerivate tingimuste juures aga kõrged (Eh 300 kuni 600 mV, pE 5 kuni 15). Vee redokspotentsiaali määravad hapnikusisaldus ja pH:
kus Po on hapniku osarõhk.
Temperatuur mõjutab redokspotentsiaali suhteliselt vähe. Praktikas arvutatakse tavaliselt Eh7, so. redokspotentsiaal pH=7 juures:
Temperatuur mõjutab redokspotentsiaali suhteliselt vähe. Praktikas arvutatakse tavaliselt Eh7, so. redokspotentsiaal pH=7 juures:
Neutraalses reaktsiooniga ja hapnikuga 100% küllastunud vees on redokspotentsiaal pisut üle 500mV, mis on märkimisväärselt väiksem kui teoreetiline 800mV. Ioonid esinevad oksüdeeritud kujul. Madala hapnikusisalduse juures (näiteks kihistunud järvede hüpolimnion) on redokspotentsiaal madal, settes isegi negatiivne ning esinevad peamiselt redutseeritud vormid. Mitmete veekogudes oluliste elementide esinemisvormi sõltumine Eh konkreetsetest väärtustest oleks järgmine: