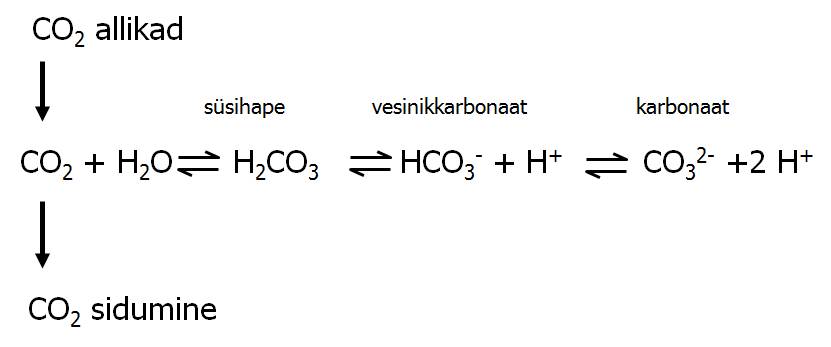Süsihappegaas
Süsihappegaasi (CO2) leidub õhus keskmiselt 0,03 mahuprotsenti ehk 0,3 ml/l. Vees lahustub normaaltingimustel aga 1 liitris 0,514 ml CO2. Temperatuuri tõustes ja soolsuse suurenedes lahustuvus vees väheneb. Süsihappegaas esineb vees peamiselt lahustunud molekulidena. Ca. 1% moodustab neist süsihappe, mis dissotsieerub (Joonis 24):
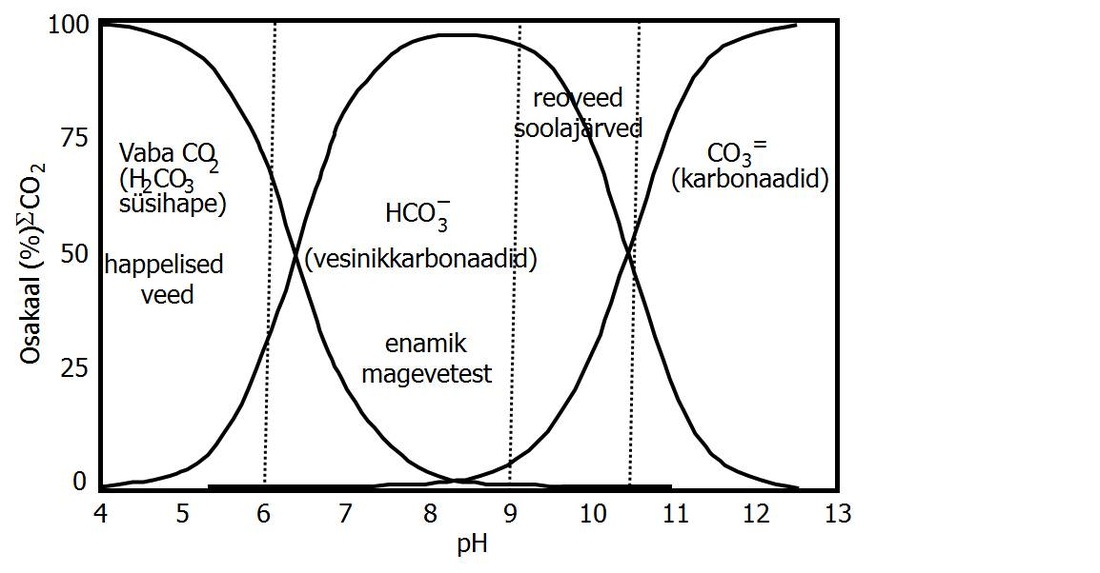
Taolises puhversüsteemis sõltub erinevate komponentide suhe vesinikioonide kontsentratsioonist (Joonis 25). Vesinikkarbonaat- ja karbonaatioonid reageerivad metallidega, andes sooli, millest loodusvetes on levinuimad magneesium- ja eriti kaltsiumkarbonaat.
Kaltsiumkarbonaat lahustub vees väga halvasti ning sete moodustub aluselise reaktsiooniga vees juba suhteliselt väikese kaltsium- ja karbonaatioonide kontsentratsiooni juures. Kui nüüd vesi muutub happelisemaks ja süsihappe dissotsiatsioonil vabanenud karbonaatioonide hulk väheneb, siis nende kadu kompenseeritakse karbonaatide lahustumisel vabanevate karbonaatioonidega. Kui keskkonna pH jääb endiselt happeliseks, seotakse karbonaatioonidega vesinikioonid ning pH tõuseb. Vajalikud karbonaatioonid saadakse täiendava karbonaatide lahustumise teel. Taoline protsess kestab niikaua, kui jätkub karbonaate või pH tõuseb piisavalt kõrgele. Vastupidine olukord tekib aluselises keskkonnas. Karbonaatioonide hulga kasvamisel seotakse need kaltsiumioonidega ning toimub kaltsiumkarbonaadi settimine. Selle käigus vabanevad vesinikioonid ja keskkond muutub happelisemaks. Sellisel kujul toimib veekogudes karbonaatne puhversüsteem, mis hoiab ära keskkonna pH muutused niikaua, kui seal leidub karbonaate või säilib kontakt atmosfääri CO2.
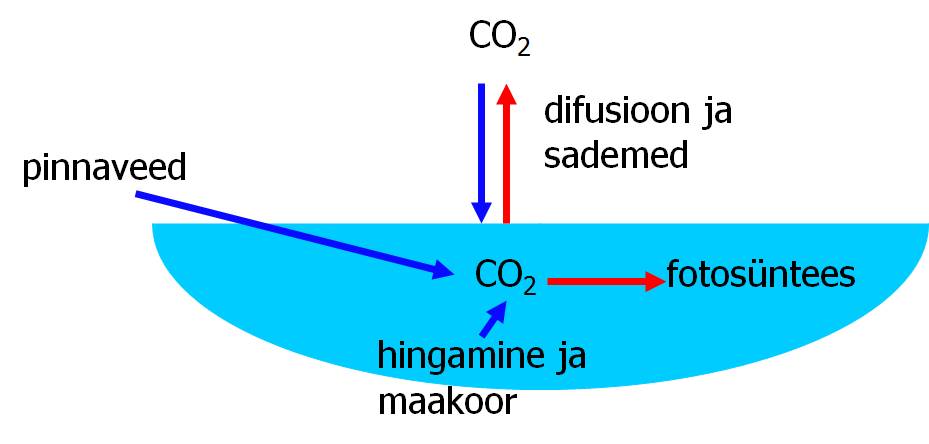
Süsihappegaasi allikaks vees (Joonis 26) on eelkõige orgaaniliste ainete oksüdatsiooniprotsessid. Mõned põhjaveed rikastuvad süsihappegaasiga, mis pärineb Maa sisemusest. Süsihappegaasi neeldumisel atmosfäärist on oluline osa ainult mere ja ookeanide puhul. CO2 partsiaalrõhk maismaavetes ületab enamasti tema partsiaalrõhu atmosfääris. Seetõttu on tasakaal suunatud CO2 lendumisele veest õhku.
Süsihappegaasi allikaks vees (Joonis 26) on eelkõige orgaaniliste ainete oksüdatsiooniprotsessid. Mõned põhjaveed rikastuvad süsihappegaasiga, mis pärineb Maa sisemusest. Süsihappegaasi neeldumisel atmosfäärist on oluline osa ainult mere ja ookeanide puhul. CO2 partsiaalrõhk maismaavetes ületab enamasti tema partsiaalrõhu atmosfääris. Seetõttu on tasakaal suunatud CO2 lendumisele veest õhku.
Süsihappegaasi tarbijatest on kõige olulisem fotosüntees. Seda kulub ka karbonaatide lahustumisel ja kivimite porsumisel. Loomadele on süsihappegaas suurtes kogustes mürgine, kuid väikestes kontsentratsioonides vajalik ainevahetuse reguleerimiseks ja mitmesuguste orgaaniliste ainete sünteesiks.
|
Loodusvete CO2 sisaldus kõigub vahemikus 0,1 mg/l kuni 1 g/l. Kõige vähem sisaldavad süsihappegaasi mineraalaineterikkad veekogud, näit. soolajärved ja ookeanid. Kõige rohkem leidub seda põhja- ja reovetes (Joonis 27). Perioodilisi ööpäevaseid muutusi põhjustab fotosüntees. Sisaldus väheneb kevadel ja suvel, kuid hakkab sügise saabudes kasvama ja saavutab maksimumi talvel. Võrreldes sesoonse amplituudiga on ööpäevane amplituud suurem.
|