Vee molekulaarsed omadused
Veel on terve rida märkimisväärseid või lausa anomaalseid omadusi. Neist tähtsamad on järgmised.
• Perioodilisussüsteemi VI rühma elementide vesinikuühendid peaksid olema kõik gaasilised. Vesi on aga Maal erandlikult leitav kolmes olekus - vedela, tahke ja gaasilisena.
• Tiheduse anomaalia. Tavaliselt on aine tihedus tahkes olekus suurem selle tihedusest vedelas olekus. Vee puhul on aga see vastupidi, jää tihedus on 0,920 g/cm³ ning vedelal veel +4°C juures aga 1,000 g/cm³. Tiheduse anomaalia tõttu ujub jää veepinnal.
• Enamik aineid paisub soojendamisel, kuid vee soojenemisel vahemikus 0°C kuni +4°C ruumala hoopis kahaneb.
• Veel on suur erisoojus - 1 cal·gˉ¹·°Cˉ¹. Sellest suurem erisoojus vaid vedelal ammoniaagil (1,23) ja vedelal vesinikul (3,4). See omadus on aluseks vesikeskkonna suurele termilisele stabiilsusele ning mõjutab kliimat, kuna vee soojusmahtuvus on 4 korda suurem kui õhul. Kõrge sulamissoojuse tõttu sulavad jää ja lumi aeglaselt.
• Vesi on suhteliselt universaalne lahusti ja tal on suur pindpinevus.
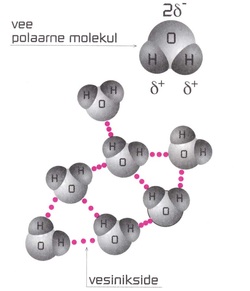
Vee unikaalsed omadused on tingitud tema molekulaarsest struktuurist. Piltlikult võiks vee molekuli kujutada võrdhaarse kolmnurgana, mille tipus asub hapnikuaatom ja alustes vesinikuaatomid (Joonis 3).
• Perioodilisussüsteemi VI rühma elementide vesinikuühendid peaksid olema kõik gaasilised. Vesi on aga Maal erandlikult leitav kolmes olekus - vedela, tahke ja gaasilisena.
• Tiheduse anomaalia. Tavaliselt on aine tihedus tahkes olekus suurem selle tihedusest vedelas olekus. Vee puhul on aga see vastupidi, jää tihedus on 0,920 g/cm³ ning vedelal veel +4°C juures aga 1,000 g/cm³. Tiheduse anomaalia tõttu ujub jää veepinnal.
• Enamik aineid paisub soojendamisel, kuid vee soojenemisel vahemikus 0°C kuni +4°C ruumala hoopis kahaneb.
• Veel on suur erisoojus - 1 cal·gˉ¹·°Cˉ¹. Sellest suurem erisoojus vaid vedelal ammoniaagil (1,23) ja vedelal vesinikul (3,4). See omadus on aluseks vesikeskkonna suurele termilisele stabiilsusele ning mõjutab kliimat, kuna vee soojusmahtuvus on 4 korda suurem kui õhul. Kõrge sulamissoojuse tõttu sulavad jää ja lumi aeglaselt.
• Vesi on suhteliselt universaalne lahusti ja tal on suur pindpinevus.
Vee unikaalsed omadused on tingitud tema molekulaarsest struktuurist. Piltlikult võiks vee molekuli kujutada võrdhaarse kolmnurgana, mille tipus asub hapnikuaatom ja alustes vesinikuaatomid (Joonis 3).
Skeemis nähtub, et sidemes -O-H on elektronpaar tõmmatud suurema elektronegatiivsusega elemendi – hapniku aatomi poole, mis omandab seetõttu negatiivse osalaengu, vesiniku aatom aga positiivse osalaengu. Seega on vee molekul polaarse ehitusega. Suure dipoolmomendi tõttu on veel suur dielektriline läbitavus, mis tingib ka hea lahustamisvõime. Vesi ei lahusta hästi mitte ainult elektrolüüte, vaid ka paljusid orgaanilistest mitteelektrolüütidest ja gaasidest.
|
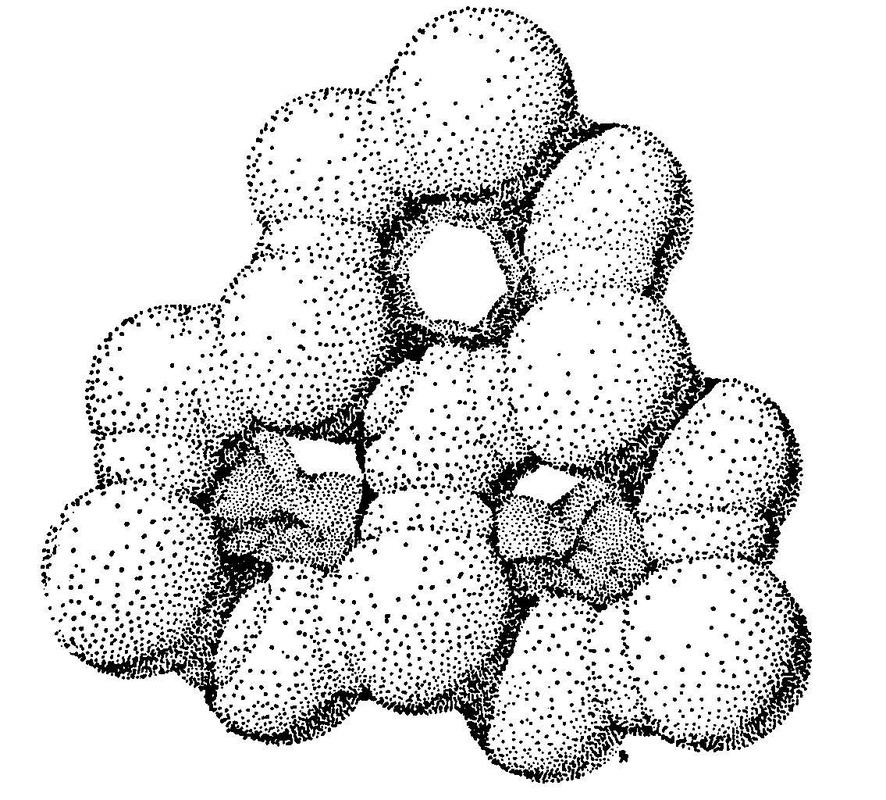
Vedelas ja tahkes olekus valitseb veemolekulide vahel vesinikside, mistõttu vee molekulid moodustavad assotsiaate (H2O)n, milles n väärtus on 2 kuni 10 (Joonis 4). Jääkristallides (Joonis 5) on iga vee molekul seotud vesiniksideme abil tetraeedriliselt nelja naabermolekuliga ning moodustab koheva ruumilise struktuuri. Selle koheva struktuuri tõttu on jää tihedus vee tihedusest väiksem. Jää tetraeedriline struktuur säilib lähikorrastatuse mõttes peale sulamist ka vees, kuid struktuuritühikute vähenemisega toimub molekulide koondumine ja vee tihedus kasvab, kuni saavutatakse temperatuur 3,98°C. Kuigivõrd vee soojenedes molekulide liikuvus küll suureneb, kuid struktuuriefekt ületab veel soojusliikumise mõju. Edasisel soojendamise üle 3,98°C on juba ülekaalus soojusliikumise mõju, molekulid eemalduvad teineteisest ja vesi hakkab paisuma. Lõplikult lõhutakse vesiniksidemete struktuur alles vee aurustumisel. 20°C juures on vesiniksidemetest alles veel pooled. Kõrge sulamissoojuse ja suure soojusmahtuvuse põhjusteks ongi energiakulu struktuuri ja kohevusastme muutumisel.
|